結核分枝桿菌
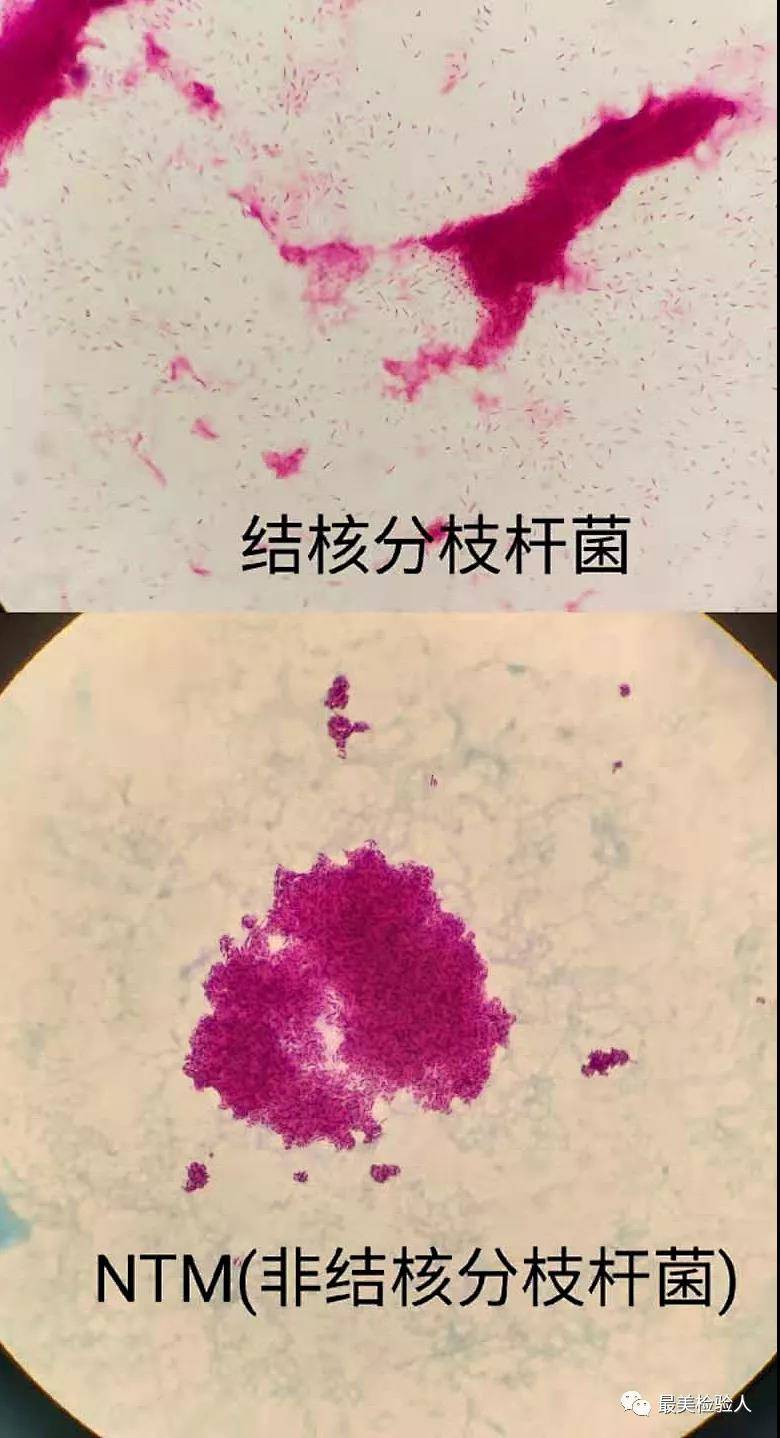 |
結核分枝桿菌(M.tuberculosis),俗稱結核桿菌(tubercle bacillus),是引起結核病的病原體。[1]1882年由德國細菌學家郭霍(Robert Koch,1843-1910)發現並證明為人類結核病的病原菌,該菌可侵犯全身各器官,但以引起肺結核最多見。結核病是一種古老的疾病,全球廣泛分布,是細菌感染性疾病致死的首位原因。
結核桿菌是需氧菌,生長緩慢,但它對乾燥、冷、酸、鹼等抵抗力也很強,在陽光直射下,痰中結核桿菌需要經過2~7小時才會被殺死。
目錄
簡介
結核分枝桿菌(M. tuberculosis)簡稱為結核桿菌(tubercle bacilli),是人類結核病的病原體。是專性需氧的一類細菌,抗酸染色陽性。無鞭毛,有菌毛,有微莢膜但不形成芽孢,其細菌壁既沒有革蘭陽性菌的磷壁酸,也沒有革蘭陰性菌的脂多糖。德國細菌學家郭霍(Robert Koch,1843-1910)於1882年發現並證明為人類結核病的病原菌。該菌感染人體導致的結核病是嚴重影響人類生命健康的一種傳染病,經過與其幾個世紀的抗爭後逐漸得到控制,但近年來由於多種因素的影響,該疾病變得日趨嚴重。
研究歷史
1882年,德國細菌學家郭霍(Robert Koch,1843-1910)首先發現並證明結核分枝桿菌是結核病的病原菌。本菌可侵犯全身各組織器官,但以肺部感染最多見。結核病嚴重影響人類健康和生命,人類與之鬥爭了許多世紀。在17-18世紀的歐洲,結核病被稱為"白色瘟疫",幾乎100%的歐洲人被感染,25%的歐洲人死亡。隨着抗結核藥物的不斷發展和衛生生活狀況的改善,結核的發病率和死亡率曾一度大幅下降。20世紀90年代以來,由於艾滋病和結核分枝桿菌耐藥菌株的出現、免疫抑制劑的應用、吸毒、貧困及人口流動等因素,全球範圍內結核病的疫情驟然惡化。結核病成為首要的再現傳染病,成為了全球尤其是發展中國家最為嚴重的全球性衛生問題。全世界約有1/3的人感染結核分枝桿菌,每年有900萬的新病例出現,有200萬人死於該疾病。
生物學性狀
形態與染色
結核分枝桿菌為細長略帶彎曲的桿菌,大小1~4X0.4μm。牛分枝桿菌則比較粗短。分枝桿菌屬的細菌細胞壁脂質含量較高,約占乾重的60%,大量分枝菌酸(mycolic acid)包圍在肽聚糖層的外面,可影響染料的穿入。分枝桿菌一般用齊尼(Ziehl- Neelsen)抗酸染色法,以5% 石炭酸復紅加溫染色後可以染上,但用3%鹽酸乙醇不易脫色。若再加用美藍復染,則分枝桿菌呈紅色,而其他細菌和背景中的物質為藍色。本菌無芽孢、無鞭毛。
結核分枝桿菌在體內外經青黴素、環絲氨酸或溶菌酶誘導可影響細胞壁中肽聚糖的合成,異煙肼影響分枝菌酸的合成,巨噬細胞吞噬結核分枝桿菌後溶菌酶的作用可破壞肽聚糖,均可導致其變為L型細菌,呈顆粒狀或絲狀。異煙肼影響分枝菌酸的合成,可變為抗酸染色陰性。這種形態多形染色多變在肺內外結核感染標本中常能見到。臨床結核性冷膿瘍和痰標本中甚至還可見有非抗酸性革蘭陽性顆粒,過去稱為Much顆粒。該顆粒在體內或細胞培養中能返回為抗酸性桿菌,故亦為L型細菌。
培養特性
專性需氧。最適溫度為37℃,低於30℃不生長。結核分枝桿菌細胞壁的脂質含量較高,影響營養物質的吸收,故生長緩慢。結核菌在含氧40%~50%並有5%~10%CO2和溫度為36℃±5℃,合適PH值為6.8~7.2的條件下生長旺盛。在一般培養基中每分裂1代需時18~24小時,營養豐富時只需5小時。
初次分離需要營養豐富的培養基。常用的有羅氏(Lowenstein-Jensen)固體培養基,內含蛋黃、甘油、馬鈴薯、無機鹽和孔雀綠等。孔雀綠可抑制雜菌生長,便於分離和長期培養。蛋黃含脂質生長因子,能刺激生長。根據接種菌多少,一般2~4周可見菌落生長。菌落呈顆粒、結節或花菜狀,乳白色或米黃色,不透明。在液體培養基中可能由於接觸營養面大,細菌生長較為迅速。一般1~2周即可生長。臨床標本檢查液體培養比固體培養的陽性率高數倍。
生化反應
結核分枝桿菌不發酵糖類。與牛分枝桿菌的區別在於結核分枝桿菌可合成煙酸和還原硝酸鹽,而牛分枝桿菌不能。熱觸酶試驗對區別結核分枝桿菌與非結核分枝桿菌有重要意義。結核分枝桿菌大多數觸酶試驗陽性,而熱觸酶試驗陰性; 非結核分枝桿菌則大多數兩種試驗均陽性。熱觸酶試驗檢查方法是將濃的細菌懸液置68℃水浴加溫20分鐘,然後再加H2O2。觀察是否產生氣泡,有氣泡者為陽性。
抵抗力
結核分枝桿菌對乙醇敏感,在70%乙醇中2分鐘死亡。此外,菌體脂質可防止菌體水分丟失,故對乾燥的抵抗力特別強。粘附在塵埃上保持傳染性8~10d,在乾燥痰內可存活6~8個月。結核分枝桿菌對濕熱敏感,在液體中加熱62~63℃ 15分鐘或煮沸即被殺死。結核分枝桿菌對紫外線敏感。直接日光照射數小時可被殺死,可用於結核患者衣服、書籍等的消毒。
結核分枝桿菌對酸(3% HCl或6% H2SO4)或鹼(4% NaOH)有抵抗力,15分鐘不受影響。可在分離培養時用於處理有雜菌污染的標本和消化標本中的粘稠物質。結核分枝桿菌對1:13 000孔雀綠有抵抗力,加在培養基中可抑制雜菌生長。
變異性
結核分枝桿菌可發生形態、菌落、毒力、免疫原性和耐藥性等變異。卡介苗(BCG)就是Calmette和Guerin (1908)將牛結核分枝桿菌在含甘油、膽汁、馬鈴薯的培養基中經13年230次傳代而獲得的減毒活疫苗株,現廣泛用於預防接種。
致病性
結核分枝桿菌不產生內、外毒素。其致病性可能與細菌在組織細胞內大量繁殖引起的炎症,菌體成分和代謝物質的毒性以及機體對菌體成分產生的免疫損傷有關。
致病物質
1.莢膜 莢膜的主要成分為多糖,部分脂質和蛋白質。其對結核分枝桿菌的作用有:①莢膜能與吞噬細胞表面的補體受體3(CR3)結合,有助於結核分枝桿菌在宿主細胞上的粘附與入侵;②莢膜中有多種酶可降解宿主組織中的大分子物質,供入侵的結核分枝桿菌繁殖所需的營養;③莢膜能防止宿主的有害物質進入結核分枝桿菌,甚至如小分子NaOH也不易進入。故結核標本用4% NaOH消化時,一般細菌很快殺死,但結核分枝桿菌可耐受數十分鐘。結核分枝桿菌入侵後莢膜還可抑制吞噬體與溶酶體的融合。
2.脂質 據實驗研究細菌毒力可能與其所含複雜的脂質成分有關,特別是糖脂更為重要。①索狀因子 :是分枝菌酸和海藻糖結合的一種糖脂。能使細菌在液體培養基中呈蜿蜒索狀排列。此因子與結核分枝桿菌毒力密切相關。它能破壞細胞線粒體膜,影響細胞呼吸,抑制白細胞遊走和引起慢性肉芽腫。若將其從細菌中提出,則細菌喪失毒力。②磷脂:能促使單核細胞增生,並使炎症灶中的巨噬細胞轉變為類上皮細胞,從而形成結核結節。③硫酸腦苷脂(sulfatide):可抑制吞噬細胞中吞噬體與溶酶體的結合,使結核分枝桿菌能在吞噬細胞中長期存活。④蠟質D:是一種肽糖脂和分枝菌酸的複合物,可從有毒株或卡介苗中用甲醇提出,具有佐劑作用,可激發機體產生遲髮型超敏反應。
3.蛋白質 結核分枝桿菌含有大量蛋白質,作為毒力因子與細菌致病性有關。結核菌素是菌體蛋白的主要成分,和蠟質D結合後能使機體發生超敏反應,引起組織壞死和全身中毒症狀,並在形成結核結節中發揮一定作用。
所致疾病
結核分枝桿菌可通過呼吸道、消化道或皮膚損傷侵入易感機體,引起多種組織器官的結核病,其中以通過呼吸道引起肺結核為最多。結核分枝桿菌可通過飛沫微滴或含菌塵埃的吸入,故肺結核較為多見。
1.肺內感染⑴原發感染:多發生於兒童。多表現為低熱,盜汗,少量咯血等症狀。肺泡中有大量巨噬細胞,少數活的結核分枝桿菌進入肺泡即被巨噬細胞吞噬。由於該菌有大量脂質,可抵抗溶菌酶而繼續繁殖,使巨噬細胞遭受破壞,釋放出的大量菌在肺泡內引起炎症,稱為原發灶。初次感染的機體因缺乏特異性免疫,結核分枝桿菌常經淋巴管到達肺門淋巴結,引起肺門淋巴結腫大和導致淋巴管炎,三者稱為原發綜合徵。其中少數患者因免疫低下,可經血和淋巴系統,播散至骨、關節、腎、腦膜及其他部位引起相應的結核病。90% 以上的原發感染形成纖維化或鈣化,不治而愈,但病灶內常仍有一定量的結核分枝桿菌長期潛伏。
⑵繼發性感染:本類型是成人最常見的類型。病灶亦以肺部為多見。多為原發潛伏病灶來源細菌導致,少數是外來源性細菌感染。主要表現為低熱,盜汗,咯血等症狀。長呈慢性發病,少數急性發作。由於免疫以及治療的差別導致出現多種不同類型的病灶。繼發性結核病病灶趨於極限,但是排菌較多,在流行病學上更為重要。
2.肺外感染 部分患者結核分枝桿菌可進入血液循環引起肺內、外播散,如腦、腎結核,痰菌被嚥入消化道也可引起腸結核、結核性腹膜炎等。
免疫性
免疫機制
結核分枝桿菌是兼性胞內寄生菌,其免疫主要是以T細胞為主的細胞免疫,CD4T細胞是主要的免疫細胞。機體對結核分枝桿菌雖能產生抗體,但此抗體無保護作用。CD4T細胞激活後釋放細胞因子刺激巨噬細胞,巨噬細胞殺傷和清除結核分枝桿菌,從而使病灶炎症消失,機體康復。病灶的清除與病灶的大小有關,病灶過大,形成纖維囊時,則巨噬細胞無法進入殺滅細菌,細菌會在病灶中進入靜息狀態,產生潛伏感染。
結核的免疫屬於感染免疫(infection immunity),又稱有菌免疫,即只有當結核分枝桿菌或其組分存在體內時才有免疫力。一旦體內的結核分枝桿菌或其組分全部消失,免疫也隨之不存在。
超敏反應
隨着機體對結核分枝桿菌產生保護作用的同時,也可以有遲髮型超敏反應的產生,二者均為T細胞介導的結果。超敏反應既與免疫機制有關,也與細菌的致病機制有關。
實驗室診斷
結核菌素試驗
結核菌素試驗(PPDtest)是應用結核菌素進行皮膚試驗來測定機體對結核分枝桿菌是否能引起超敏反應的一種試驗。
常規試驗分別取2種PPD 5個單位注射兩前臂皮內,48~72h後紅腫硬結超過5mm者為陽性,≥15mm為強陽性,對臨床診斷有意義。若PPD-C側紅腫大於BCG-PPD側為感染。反之,BCG-PPD側大於PPD-C側,可能系卡介苗接種所致。
陰性反應表明未感染過結核分枝桿菌,但應考慮以下情況:①感染初期,因結核分枝桿菌感染後需4周以上才能出現超敏反應;②老年人;③嚴重結核患者或正患有其他傳染病,如麻疹導致的細胞免疫低下;④獲得性細胞免疫低下,如艾滋病或腫瘤等用過免疫抑制劑者。為排除假陰性,國內有的單位加用無菌植物血凝素(PHA)針劑 ,0.1ml含10μg作皮試。若24h紅腫大於PHA皮丘者為細胞免疫正常,若無反應或反應不超過PHA皮丘者為免疫低下。
結核菌γ干擾素釋放試驗
細胞免疫介導的結核菌γ干擾素釋放試驗(T-cell interferon gamma release assays,TIGRA,又稱IFNGRA或GRA)是近年來採用酶聯免疫吸附測定(ELISA)或酶聯免疫斑點(ELISPOT)法定量檢出受檢者全血或外周血單個核細胞對結核分枝桿菌特異性抗原的IFN-γ檢測釋放反應,用於結核菌潛伏感染的診斷。IFN-γ為Th1細胞分泌的一種細胞因子,不但能夠反映機體結核的Th1細胞免疫情況,還與體內結核菌的抗原含量密切相關。被結核分枝桿菌抗原致敏的T細胞再遇到同類抗原時能產生高水平的IFN-γ,因此被用於結核潛伏感染的診斷。特異性強於PPD。
直接塗片鏡檢
標本直接塗片或集菌後塗片,用抗酸染色。若找到抗酸陽性菌即可初步診斷。抗酸染色一般用Ziehl-Neelsen法。為加強染色,可用IK(intensified Kinyoun)法染色。將石炭酸復紅染色過夜,用0.5% 鹽酸乙醇脫色30s,則包括大多結核分枝桿菌L型也可着色。為提高鏡檢敏感性,也可用金胺染色,在熒光顯微鏡下結核分枝桿菌呈顯金黃色熒光。
分離培養
將經中和集菌材料接種於固體培養基,器皿口加橡皮塞於37℃培養,每周觀察1次。結核分枝桿菌生長緩慢,一般需2~4周長成肉眼可見的落菌。液體培養可將集菌材料滴加於含血清的培養液,則可於1~2周在管底見有顆粒生長。取沉澱物作塗片,能快速獲得結果,並可進一步作生化、藥敏等測定和區分結核分枝桿菌與非結核分枝桿菌。國內學者已證明結核分枝桿菌L型可存在於血細胞內或粘附於細胞表面。這種患者往往血沉加快,用低滲鹽水溶血後立即接種高滲結核分枝桿菌L型培養基能提高培養陽性率。
動物試驗
將集菌後的材料注射於豚鼠腹股溝皮下,3~4周後若局部淋巴結腫大,結核菌素試驗陽轉,即可進行解剖。觀察肺、肝、淋巴結等器官有無結核病變,並作形態、培養等檢查。若6~8周仍不見發病,也應進行解剖檢查。
快速診斷
一般塗片檢查菌數需5x103~4/ml,培養需1x102/ml,標本中菌數少於此數時不易獲得陽性結果,且培養需時較長。應用多聚酶鏈反應(PCR)擴增技術應用於結核分枝桿菌DNA鑑定,每ml中只需含幾個細菌即可獲得陽性,且1-2d得出結果。操作中需注意實驗器材的污染問題,以免出現假陽性。又細菌L型由於缺壁並有代償性細胞膜增厚,而一般常用的溶菌酶不能使細胞膜破裂釋出DNA,以致造成PCR假陰性。用組織磨碎器充分研磨使細胞破裂後,則可出現陽性。有條件的單位使用BACTEC法,以含14C棕櫚酸作碳源底物的7H12培養基,測量在細菌代謝過程中所產生的14C量推算出標本中是否有抗酸桿菌,5~7d就可出報告。
防治原則
預防
近20年國際組織提出控制結核病主要方法有:發現和治療痰菌陽性者在傳染源上進行防控。卡介苗(BCG)接種。目前較普遍的看法是接種後尚不足以預防感染,但可以顯著降低新生兒發病及嚴重性。
Dots戰略是who根據20年來的經驗將其上升為一種保證結核病控制對策獲得成功的戰略。
治療
目前結核病治療主要以藥物化療為主。利福平、異煙肼、乙胺丁醇、鏈黴素,吡嗪酰胺等為一線抗結核藥物。藥物失敗或者危及生命的局限性病變等可以採取手術治療。治療中重要的還有對症治療,例如發熱的治療,咯血的防治等。[2]