電解池檢視原始碼討論檢視歷史
| 電解池 |
 |
電解池的主要應用用於工業制純度高的金屬,是將電能轉化為化學能的一個裝置(構成:外加電源,電解質溶液,陰陽電極)。使電流通過電解質溶液或熔融電解質而在陰,陽兩極引起還原氧化反應的過程。
簡介
基本概念 (1)使電流通過電解質溶液或熔融的電解質而在陰、陽兩極上引起還原氧化反應的過程叫做電解。
(2)把電能轉變為化學能的裝置叫做電解池或電解槽。
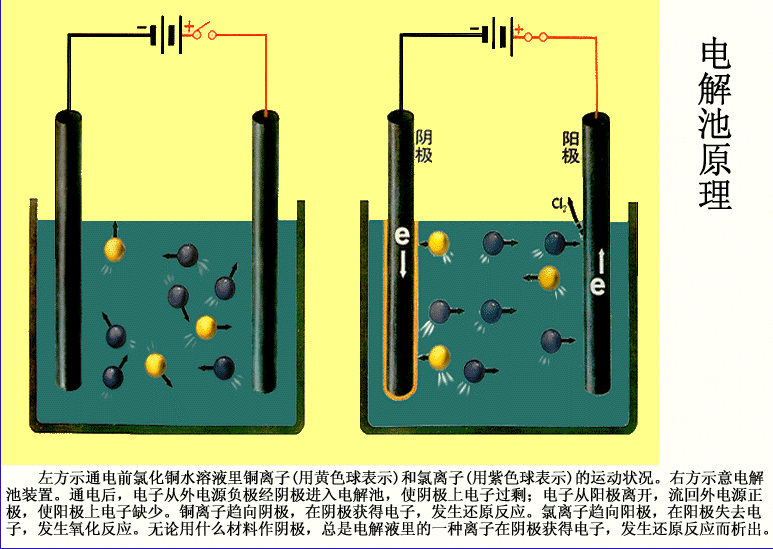
(3)當離子到達電極時,失去或獲得電子,發生氧化還原反應的過程電解原理(電解池裝置如圖)
陰極:與電源負極相連的電極。(得電子發生還原反應)
陽極:與電源正極相連的電極。(失電子發生氧化反應)
電解定義 電解是使電流通過電解質溶液(或者是熔融的電解質)
而在陰、陽兩極引起還原氧化反應的過程。
上圖是電解CuCl2溶液的裝置。
通電後發生反應:
CuCl2=(電解)Cu+Cl2
陽極:2Clˉ - 2e- → Cl2 ↑
陰極:Cu2- + 2e- -→ Cu
電解過程中的能量轉化(裝置特點)一定不參與反應 不一定是惰性電極陽極:不一定參與反應 也不一定是惰性電極
反應條件 ①連接直流電源
②陰陽電極 陰極:與電源負極相連為陰極
陽極:與電源正極相連為陽極
③兩極處於電解質溶液或熔融電解質中
④兩電極形成閉合迴路
電極反應 電極反應與電源的正極相連的電極稱為陽極。
物質在陽極上失去電子,發生氧化反應。如上圖裝置中,Cl在陽極上失去電子轉化為Cl2,陽極反應式:2Cl -2e=Cl2↑簡記為陽氧。
與電源的負極相連的電極成為陰極。
物質在陰極上得到電子,發生還原反應。如上圖裝置中,Cu在陰極是得到電子轉化為Cu,陰極反應式:Cu+2e→Cu簡記為陰原(陰原)
電解結果 在兩極上有新物質生成
反應規律 陽極:活潑金屬-電極失電子(Au,Pt除外);
惰性電極-溶液中陰離子失電子
失電子能力:活潑金屬(除Pt,Au)>S>I>Br>Cl>OH>含氧酸根(NO>SO4)>F
陰極:溶液中陽離子得電子能力:Ag>Hg>Fe>Cu>H(酸)>Pb>Sn>Fe>Zn>H(水)>Al>Mg>Na>Ca>K(即金屬活潑性順序表的逆向)
規律:鋁前(含鋁)離子不放電,氫(酸)後離子先放電,氫(酸)前鋁後的離子看條件。
四類電解型的電解規律(當陽極為惰性電極時)
①電解水型(強鹼,含氧酸,活潑金屬的含氧酸鹽),pH由溶液的酸鹼性決定,溶液呈鹼性則pH增大,溶液呈酸性則pH減小,溶液呈中性則pH不變。電解質溶液復原-加適量水。
②電解電解質型(無氧酸,不活潑金屬的無氧酸鹽),無氧酸pH變大,不活潑金屬的無氧酸鹽pH不變。電解質溶液復原-加適量電解質。
③放氫生鹼型(活潑金屬的無氧酸鹽),pH變大。電解質溶液復原-加陰離子相同的酸。
④放氧生酸型(不活潑金屬的含氧酸鹽),pH變小。電解質溶液復原-加陽離子相同的鹼或氧化物。
電解意義 使在通常情況下不發生變化的物質發生氧化還原反應,得到所需的化工產品、進行電鍍以及冶煉活潑的金屬,在金屬的保護方面也有一定的用處。
評價
注意事項
1.無氧酸是其本身的電解
2.含氧酸是水的電解
3.可溶性鹼是水的電解
4.活潑性金屬的含氧酸鹽也是水的電解
5.活潑金屬的無氧鹽陰極析出氫氣並伴隨溶液顯鹼性,陽極析出非金屬單質
6.不活潑金屬的無氧鹽是該鹽的電解
7.中等活動性金屬的含氧酸鹽陰極析出金屬,陽極得到氧氣同時酸性提高
記憶方法
陽極出氧鹵,陰極氫金屬。
鹽的離子都放電,離子濃度急速減;
鹽的離子不放電,水耗離子濃度添。
酸根離子單放電,產物必得鹵氫鹼;
金屬離子單放電,產物必得含氧酸。[1]