呼吸鏈檢視原始碼討論檢視歷史
| 呼吸鏈 |
 |
呼吸鏈(respiratory chain)是由一系列的遞氫反應(hydrogen transfer reactions)和遞電子反應(electrontransfer reactions)按一定的順序排列所組成的連續反應體系,它將代謝物脫下的成對氫原子交給氧生成水,同時有ATP生成。實際上呼吸鏈的作用代表着線粒體最基本的功能,呼吸鏈中的遞氫體(hydrogen carrier)和遞電子體(electron carrier)就是能傳遞氫原子或電子的載體,由於氫原子可以看作是由質子和核外電子組成的,所以遞氫體也是遞電子體,遞氫體和遞電子體的本質是酶、輔酶、輔基或輔因子。
簡介
呼吸鏈又稱電子傳遞鏈,是由一系列電子載體構成的,從NADH或FADH2向氧傳遞電子的系統。
還原型輔酶通過呼吸鏈再氧化的過程稱為電子傳遞過程。其中的氫以質子形式脫下,電子沿呼吸鏈轉移到分子氧,形成粒子型氧,再與質子結合生成水。放出的能量則使ADP和磷酸生成ATP。電子傳遞和ATP形成的偶聯機制稱為氧化磷酸化作用。整個過程稱為氧化呼吸鏈或呼吸代謝。
在葡萄糖的分解代謝中,一分子葡萄糖共生成10個NADH和2個FADH2,其標準生成自由能是613千卡,而在燃燒時可放出686千卡熱量,即90%貯存在還原型輔酶中。呼吸鏈使這些能量逐步釋放,有利於形成ATP和維持跨膜電勢。
原核細胞的呼吸鏈位於細胞質膜上,真核細胞則位於線粒體內膜上。
評價
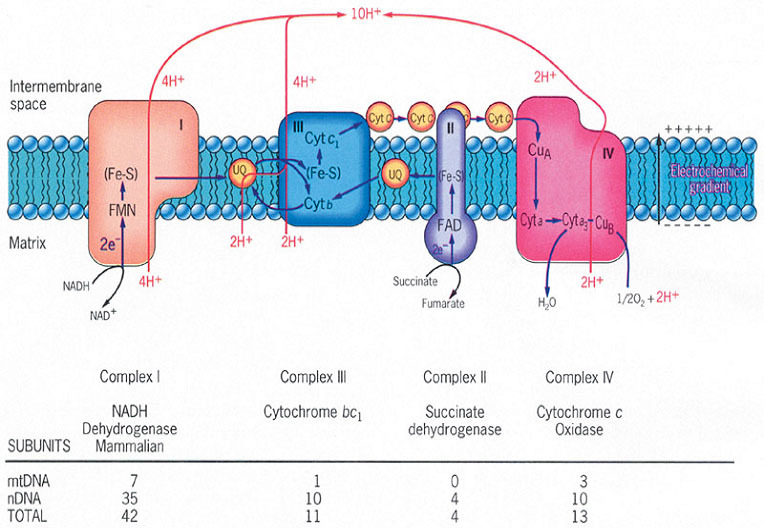
呼吸鏈包含15種以上組分,主要由4種酶複合體和2種可移動電子載體構成。其中複合體Ⅰ、Ⅱ、Ⅲ、Ⅳ、輔酶Q和細胞色素C的數量比為1:2:3:7:63:9。
複合體Ⅰ 即NADH,輔酶Q氧化還原酶複合體,由NADH脫氫酶(一種以FMN為輔基的黃素蛋白)和一系列鐵硫蛋白(鐵-硫中心)組成。它從NADH得到兩個電子,經鐵硫蛋白傳遞給輔酶Q。鐵硫蛋白含有非血紅素鐵和酸不穩定硫,其鐵與肽類半胱氨酸的硫原子配位結合。鐵的價態變化使電子從FMNH2轉移到輔酶Q。
複合體Ⅱ 由琥珀酸脫氫酶(一種以FAD為輔基的黃素蛋白)和一種鐵硫蛋白組成,將從琥珀酸得到的電子傳遞給輔酶Q。
輔酶Q 是呼吸鏈中唯一的非蛋白氧化還原載體,可在膜中迅速移動。它在電子傳遞鏈中處於中心地位,可接受各種黃素酶類脫下的氫。複合體Ⅲ 輔酶Q:細胞色素C氧化還原酶複合體,是細胞色素和鐵硫蛋白的複合體,把來自輔酶Q的電子,依次傳遞給結合在線粒體內膜外表面的細胞色素C。
細胞色素類 都以血紅素為輔基,紅色或褐色。將電子從輔酶Q傳遞到氧。根據吸收光譜,可分為三類:a,b,c。呼吸鏈中至少有5種:b、c1、c、a、a3(按電子傳遞順序)。細胞色素aa3以複合物形式存在,又稱細胞色素氧化酶,是最後一個載體,將電子直接傳遞給氧。從a傳遞到a3的是兩個銅原子,有價態變化。
複合體Ⅳ:細胞色素C氧化酶複合體。將電子傳遞給氧。[1]